Э.Д. Исагулян (1), Е.В. Екушева (2), А.В. Артеменко (3), А.В. Сергеев (4), В.В. Осипова (3,5)
(1) ФГАУ НИИ нейрохирургии им. акад. Н.Н. Бурденко Минздрава России, Москва, Россия; (2) Кафедра нервных болезней ФГОУ ДПО Институт повышения квалификации ФМБА, Москва, Россия; (3) НИО неврологии Научно-технологического парка биомедицины ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России, Москва, Россия; (4) Кафедра неврологии и нейрохирургии ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России, Москва, Россия; (5) ГБУЗ Научный психоневрологический центр им. З.П. Соловьева Департамента здравоохранения г. Москвы, Россия
Контакты: Исагулян Эмиль Давидович; emisagulyan@gmail.com
Нейромодуляция (НМ) широко используется для лечения рефрактерных первичных цефалгий, хронической мигрени (ХМ) и хронической кластерной головной боли (ХКГБ), в частности. В статье приведен обзор инвазивных и неинвазивных методов НМ, рассматриваются показания и возможные механизмы их эффективности при ХМ и ХКГБ.
DOI: 10.25731/RASP.2018.03.012
Ключевые слова: нейромодуляция, показания, методы, первичные головные боли, рефрактерные головные боли, хроническая мигрень, хроническая кластерная головная боль.
NEUROMODULATION IN THE TREATMENT OF PRIMARY HEADACHE DISORDERS: MECHANISMS OF EFFICACY, METHODS AND INDICATIONS
E.D. Isagulyan (1), E.V. Ekusheva (2), A.R. Artemenko (3), A.V. Sergeev (4), V.V. Osipova (3,5)
(1) Research Institute of Neurosurgery named after N.N.Burdenko, Ministry of Health of the Russian Federation, Moscow, Russia; (2) Department of Neurology, Advanced Training Institute of the Federal Medical Biological Agency, Russia, Moscow, Russia; (3) Neurological Research Department, Research-Technological Park of Biomedicine, First Moscow State Medical University, Ministry of Health of the Russian Federation, Moscow, Russia; (4) Department of Neurology and Neurosurgery, First Moscow State Medical University, Ministry of Health of the Russian Federation, Moscow, Russia; (5) Moscow Research Clinical Centre for Neuropsychiatry, Moscow Health Department, Moscow, Russia
Neuromodulation (NM) is widely used for the treatment of refractory primary headache disorders, chronic migraine (CM) and chronic cluster headache (CCH) in particular. In the article the review of invasive and non-invasive NM methods, possible mechanism of action and the indications for NM in refractory CM and CCH are presented.
DOI: 10.25731/RASP.2018.03.012
Keywords: neuromodulation, indications, methods, primary headaches, refractory headaches, chronic migraine, chronic cluster headache.
Contact: E.D. Isagulyan; emisagulyan@gmail.com
Несмотря на быстрое развитие медицины, значительный прогресс в фундаментальных знаниях и изобретение новых методов терапии, остается немало неврологических заболеваний, в лечении которых достигнут лишь временный эффект или лечение оказывается неэффективным вовсе. Это обусловливает необходимость поиска новых препаратов и технологий, расширяющих возможности врачей при ведении трудных пациентов с заболеваниями нервной системы.
История развития и определение понятия «нейромодуляция»
Одним из перспективных и активно развивающихся направлений в медицине является высокотехнологичная нейромодуляция, позволяющая помочь больным после многолетних безуспешных попыток разнообразного и комплексного лечения. Термины «нейромодуляция» (НМ) и «нейростимуляция» (НС) часто используются как синонимы. В то же время термин «нейромодуляция» является более общим и как хирургический метод лечения боли включает в себя НС и интратекальное введение лекарственный средств. Хотя термин «НС» подразумевает только активацию, на самом деле при воздействии электрического стимула происходит как активация, так и деактивация (нейрофизиологическая блокада) сложных нейронных сетей в структурах, отвечающих за формирование боли.
Нейрофизиологический механизм НМ состоит в терапевтическом изменении функциональной активности центральной, периферической или вегетативной нервной системы путем модулирования процессов возбуждения или торможения в нейрональных системах и их элементах, посредством электрических или фармакологических воздействий с использованием специальных, в том числе имплантируемых, устройств.
Первые исследования в этом направлении начались в 60-х гг. XX в., когда была показана возможность модификации функциональной активности центральной нервной системы (ЦНС) без необратимых деструктивных воздействий на ее структурные элементы [1]. В частности, в 1961 г. впервые была успешно применена электростимуляция малоберцового нерва для улучшения функции стопы у пациента после ишемического инсульта [2], позднее названная методом функциональной электростимуляции. В 1967 г. впервые имплантированы стимулирующие электроды в эпидуральное пространство области задних столбов спинного мозга для купирования труднокурабельного болевого синдрома [3]. Дальнейшие исследования с применением этой методики показали положительный эффект в отношении спинальной спастичности [4]. В 90-х гг. XX в. была создана математическая модель нейростимуляционного лечения, появились двухэлектродные имплантируемые системы для длительного применения, расширились возможности программирования функциональных устройств и были определены первые показания к их применению.
Дальнейшее развитие метода НМ привело к значительному расширению спектра его воздействия на нервную систему: от изменения функциональной активности на уровне периферического нерва до модуляции процессов возбуждения и торможения в области сенсомоторной коры головного мозга [5]. Неинвазивность или минимальная инвазивность, высокая управляемость и обратимость воздействий на нервную систему обусловливают возможность применения методов НМ при различных заболеваниях нервной системы: при экстрапирамидной патологии (болезнь Паркинсона, синдром Туретта, эпилепсия, дистония и т.д), спастичности различного генеза (рассеянный склероз, детский церебральный паралич, травматическое или сосудистое поражение ЦНС), а также при хронических болевых синдромах, резистентных к другим видам терапии [6–8]. В последние годы различные методики этого биотехнологического направления широко используются в кардиологии, ангиологии, психиатрии, гастроэнтерологии, урологии и других областях медицины [7].
На сегодняшний день одним из перспективных направлений для применения НМ являются хронические болевые синдромы, рефрактерные к другим методам лечения. Это обусловлено тем, что, несмотря на появление новых медицинских технологий, значительное число этих пациентов остаются нечувствительными к любым видам лечения, что во всем мире представляет собой значительную медико-социальную проблему [9]. В первую очередь речь идёт о пациентах с тригеминальной и постгерпетической невралгией, с комплексным региональным болевым синдромом, с посттравматической невропатией периферических нервов, с соматогенными (онкологическими) болями [5, 8].
Одной из перспективных сфер применения НМ являются фармакорезистентные (рефрактерные) формы первичной головной боли (ГБ) хронического течения. Наибольшую проблему в практическом плане представляют две клинические разновидности: хроническая /рефрактерная мигрень (ХМ, рХМ), в том числе сочетающаяся с лекарственно-индуцированной головной болью (ЛИГБ), и хроническая/рефрактерная кластерная головная боль (ХКГБ, рХКГБ) [10]. У этих пациентов даже многократные попытки адекватной терапии с использованием средств и методик, обладающих клинически доказанной эффективностью в профилактике ХМ и ХКГБ, не приводят к успеху.
Методы НМ, применяемые при первичных цефалгиях, и предполагаемые механизмы их действия
Методы НМ, применяющиеся у пациентов с цефалгиями, подразделяют в зависимости от локализации воздействия/места имплантации (периферическая или центральная нервная система) и от степени инвазивности (неинвазивные и инвазивные) (табл. 1).
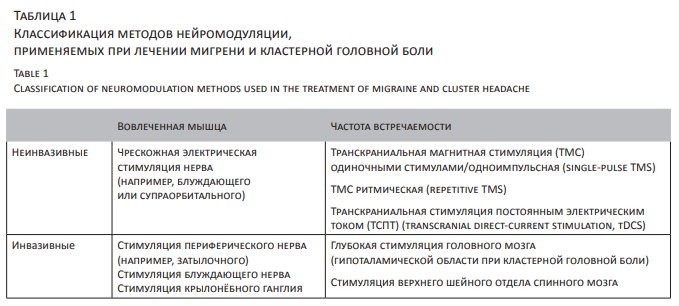
Предполагаемые механизмы действия упомянутых методов включают: 1) ингибирование патологической активности ядер гипоталамуса и таламуса путем опосредованного воздействия на них через тригеминоваскулярную систему и систему тригеминоцервикального комплекса (при электрической стимуляции (ЭС) периферических нервов или верхнего шейного отдела спинного мозга) или непосредственного воздействия на эти ядра (при глубокой стимуляции мозга, ГСМ, DBS, англ. deep brain stimulation); 2) активацию нисходящих антиноцицептивных влияний; 3) модулирующее влияние на нейрональную кортикальную возбудимость (при неинвазивных транскраниальных воздействиях методами магнитной стимуляции (ТМС) и электрической стимуляции постоянным током (ТСПТ).
Периферическая стимуляция оказывает влияние непосредственно на периферические нервы, вызывая функциональный блок проведения, зависящий от частоты стимуляции. Дополнительным механизмом является сегментарное воздействие: афферентные сенсорные Aβ-волокна блокируют сегментарную передачу ноцицептивных импульсов от Aδ- и С-волокон [11, 12]. Известно, что ноцицептивные волокна затылочного и тройничного нервов входят в состав тригеминоцервикального комплекса, что обеспечивает функциональную связь нейронов задних рогов верхних шейных сегментов (С1–С3) с каудальным ядром тройничного нерва иприводит к двунаправленной трансмиссии ноцицептивных сигналов между шеей и рецептивными полями тройничного нерва на лице и голове [13].
Эти анатомические особенности объясняют распространение боли из шейной в лобную область и наоборот, что часто отмечается у пациентов с первичными ГБ. Кроме того, активация восходящих нейронов второго порядка может оказывать модулирующий эффект на околоводопроводное серое вещество (ОСВ), что вызывает последовательную активацию нисходящих антиноцицептивных структур [14]. Это, в свою очередь, приводит к усилению ингибирования болевых импульсов и к уменьшению боли [15].
При использовании методик центральной НМ, главным образом, включаются механизмы модуляции сложной сети областей мозга, участвующих в формировании ноцицептивных и антиноцицептивных импульсов, в направлении «сверху вниз» путем стимуляции региона-мишени [5, 16]. При исследовании влияния глубокой стимуляции мозга (ГСМ) в области заднего гипоталамуса с применением позитронно-эмиссионной томографии (ПЭТ) были выявлены модулирующие эффекты на большую часть структур, входящих в «болевую матрицу» (в первую очередь серое вещество гипоталамуса и тригеминальный ганглий на стороне расположения стимулирующего электрода) [17]. Учитывая результаты, полученные с помощью ПЭТ, а также на основании наблюдения, что клинический эффект может наступить через несколько недель или месяцев после процедуры НМ, выдвинуто предположение, что в основе эффектов стимуляции лежат комплексные многоуровневые нейропластические изменения [18, 19].
Таким образом, методы центральной НМ реализуют свой эффект путем модуляции функциональной активности нейрональных структур в «нисходящем направлении» или «сверху вниз»; в то время как в основе методов периферической стимуляции лежат в первую очередь локальные или сегментарные механизмы, и «вектор модуляции» направлен «снизу вверх» [20].
Неинвазивная НМ при первичных цефалгиях
Примерами неинвазивной НМ у пациентов с ХМ/рХМ являются чрескожная стимуляция (ЧС) блуждающего нерва на шейном уровне, супраорбитального, супратрохлеарного нервов и ЧС субокципитальной зоны, а также транскраниальная магнитная стимуляция (ТМС) затылочной области (зрительной коры) одиночными стимулами, что позволяет купировать приступ мигрени (М) (при условии выполнения в течение 1 часа после начала ауры/приступа). С целью профилактического лечения применяется ритмическая ТМС (рТМС) в виде подачи повторных магнитных стимулов над головой пациента (например, высокочастотная рТМС левой префронтальной коры; низкочастотная рТМС правой дорсолатеральной префронтальной коры), что предотвращает повторение приступов и объясняется длительными пластическим эффектами после окончания стимуляции [21]. Полагают, что указанные методы позволяют снизить возбуждение в структурах «мигренозного матрикса», в первую очередь, в афферентах тригеминоваскулярной системы, тем самым снижая вероятность развития приступов М [16, 22].
Чрескожная стимуляция блужающего нерва
Чрескожная стимуляция блужающего нерва по современным данным оказывает активирующее или ингибирующее влияние на многие структуры ЦНС: таламус, структуры лимбической системы, ядро солитарного тракта, голубое пятно, церебральную кору, каудальную часть ядра спинального тракта и задние рога [11, 23, 24]. Есть данные о снижении содержания глутамата в ядрах глутаматергических нейронов тройничного нерва, возникающем в ответ на ЧС [12].
ЧС супраорбитального и супратрохлеарного нервов
Среди возможных механизмов противоболевого эффекта ЧС при профилактическом лечении ХМ обсуждаются ингибирование восходящей ноцицептивной трансмиссии и модуляция ноцицептивной активности в нейронах тригеминального ядра [23]. Использование ЧС у здоровых испытуемых было сопряжено с выраженным седативным эффектом, что расценивается как свидетельство влияния процедуры на функциональную активность структур головного мозга [25].
Транскраниальная магнитная стимуляция (ТМС) также влияет на процессы гипервозбудимости, прежде всего, подавляя процессы корковой распространяющейся депрессии, что создает предпосылки для использования этого метода для купирования острой мигренозной боли преимущественно у пациентов с М с аурой [22].
Применение рТМС приводит к снижению частоты и интенсивности приступов М в течение определенного периода времени, что напрямую зависит от параметров стимуляции: интенсивности, частоты подаваемых стимулов и локализации зоны воздействия [23, 26]. Так, рТМС стимулами низкой интенсивности, вероятно, стимулирует низкопороговые ингибиторные интернейроны, тогда как рТМС стимулами высокой интенсивности возбуждает проекционные нейроны. В зависимости от частоты рТМС можно вызвать либо долговременную потенциацию, либо длительный эффект подавления активности: высокочастотная рТМС повышает, а низкочастотная снижает кортикальную возбудимость [27]. После рТМС у пациентов с М отмечается нормализация габитуации и снижение нейрональной возбудимости – феномены, выявляемые при лечении профилактическими средствами с доказанной эффективностью: амитриптилином, бета-блокаторами, противоэпилептическими препаратами. Обсуждается влияние рТМС на высвобождение эндорфина, гиппокампального дофамина и глютамата [27].
Эффект транскраниальной стимуляции постоянным током (ТСПТ, tDCS, англ. transcranial direct current stimulation) отмечен в небольшом числе наблюдений у больных с первичными ГБ и в небольшом плацебо-контролируемом исследовании у пациентов с ХМ [28]. Основной эффект ТСПТ связан с субпороговым изменением трансмембранного потенциала при использовании тока низкой плотности, что меняет скорость развития и распространения импульса и модулирует нейрональную возбудимость. Так, при анодной стимуляции кортикальная возбудимость возрастает, а при катодной – подавляется. Также в развитии эффектов ТСПТ обсуждается роль глутаматергических NMDA-рецепторов и повышение порога болевой чувствительности у пациентов с хронической болью [14].
Инвазивная НМ при первичных цефалгиях
Периферическая инвазивная НМ
Стимуляция затылочного нерва (СЗН). Первым показанием для проведения СЗН (ONS, англ. occipital nerve stimulation) была невралгия затылочного нерва [29, 30]. В последние годы одним из основных показаний для применения этого метода является ХМ, рефрактерная к другим видам адекватной профилактической терапии (рХМ) [30]. Наиболее широко используется метод инвазивной СЗН (с имплантацией электрода подкожно в непосредственной близости от места выхода нерва с одной или двух сторон).
В связи с тяжелой дезадаптацией наибольшее количество разнообразных методов функциональной НМ используются у пациентов с хронической КГБ (ХКГБ), особенно при её рефрактерном течении [23, 26, 31–33]. Эффективность инвазивной СЗН у этой категории пациентов продемонстрирована во многих работах последних лет [23, 26, 31, 32].
Имеются данные об эффективности СЗН при других тригеминальных вегетативных цефалгиях (ТВЦ): хронической пароксизмальной гемикрании, «гемикрании континуа», синдроме КОНКС (SUNCT) и SUNA, а также при новой ежедневной персистирующей головной боли (НЕПГБ) [26, 29, 34, 35].
Стимуляция крылонебного ганглия. Одним из наиболее поздних достижений НМ в лечении рефрактерных цефалгий является стимуляция крылонебного ганглия (КГ) [36]. Основным показанием для этого метода является рХКГБ, где он может быть использован как для купирования приступа, так и в качестве профилактической терапии [37].
Другие черепно-мозговые нервы также могут быть мишенью для чрескожной стимуляции, как например, надглазничный нерв при лечении КГБ и аурикулотемпоральный (ушно-височный) нерв при лечении ХМ; есть данные об эффективности комбинированной стимуляции затылочного и надглазничного нервов у пациентов с ХМ [19].
Центральная инвазивная НМ
Стимуляция глубинных структур мозга или глубокая стимуляция головного мозга (ГСМ, DBS), а именно области заднего гипоталамуса, используется в профилактическом лечении ХКГБ и других ТВЦ с 2001 г., после того как были получены данные структурной и функциональной нейровизуализации и исследований гормонального спектра, свидетельствующие о ключевой роли этой области мозга в патофизиологии КГБ (в частности, в регуляции суточных и циркадианных ритмов) [23, 38]. В связи с риском осложнений ГСМ применяется существенно реже, чем СЗН или стимуляция крылонебного узла [23, 39, 40]. Поэтому перед принятием решения о применении ГСМ необходим тщательный отбор пациентов. Анализ показаний и критериев включения должен осуществляться междисциплинарной командой, состоящей из высококвалифицированных специалистов, в первую очередь цефалголога и нейрохирурга. Кроме того, ГС гипоталамуса должна осуществляться только в нейрохирургических центрах с достаточным опытом проведения стереотаксических операций.
Согласно рекомендациям Европейской федерации головной боли, ГСМ следует использовать исключительно у фармакорезистентных пациентов, соответствующих критериям применения этого метода [41] и только при неэффективности других методов НМ [40–42].
Описано успешное применение ГСМ у пациентов с пароксизмальной гемикранией, синдромом SUNCT, кластерной головной болью [35, 42–47]. Патофизиологические механизмы, лежащие в основе эффективности ГСМ, полностью не изучены; среди ведущих ученых обсуждается модулирующее влияние НС на механизмы нейропластичности [18].
Отбор пациентов для проведения НМ: кому и когда?
Перед принятием решения о целесообразности применения методов неинвазивной и инвазивной НМ необходимо, во-первых, удостовериться в том, что ГБ у пациента отвечает диагностическим критериям первичной цефалгии (мигрень или КГБ) в соответствии с МКГБ-3 [48]. Во-вторых, что ГБ является хронической (то есть имеет ежедневный или почти ежедневный характер) и, наконец, что ГБ является устойчивой к фармакотерапии. Следовательно, основное показание для проведения инвазивной НМ у пациентов с первичными цефалгиями – устойчивость (рефрактерность) [10, 49] болевого синдрома к повторным курсам адекватной специфической профилактической терапии и другим методам лечения.
В то же время подчеркивается, что при подозрении на рефрактерность болевого синдрома, сроки консервативного лечения не должны быть слишком продолжительными, а поздно начатая НМ дает существенно более низкие результаты, нежели проведенная своевременно. Кроме того, фармакотерапия нередко сопряжена с побочными эффектами, которые не характерны для физического воздействия в виде электрического влияния на структуры нервной системы [17].
Критерии включения для инвазивной НМ
После соответствия критериям рефрактерной цефалгии [50, 51] должны быть удовлетворены критерии включения для применения инвазивного метода НМ (табл. 2). Поскольку хронические первичные ГБ имеют тенденцию к изменению с течением времени и даже ремиссии, рекомендуется оценить двухлетний анамнез по дневникам пациента. Дополнительным критерием является наличие значительной психосоциальной дезадаптации пациента в связи с ГБ. Для оценки степени дезадаптации применяются анкета Оценка дезадаптации при мигрени (MIDAS, англ. migraine disability assessment scale) и/или опросник влияния ГБ на повседневную активность (HIT-6, англ. headache impact test) [50]. Подчеркивается, что отбор пациентов/анализ критериев включения для НМ и последующее после имплантации устройства наблюдение должно осуществляться цефалгологами – специалистами по диагностике и лечению ГБ предпочтительно на базе специализированного центра боли/ГБ [10], а оперативное вмешательство должно проводиться нейрохирургической командой, имеющей опыт инвазивной НМ [17].

НМ и коморбидные нарушения. При решении вопроса о назначении инвазивной НМ следует принимать во внимание наличие лекарственного абузуса (злоупотребление анальгетиками, в том числе триптанами) – одного из основных факторов хронизации ГБ. Поскольку у пациентов с ХМ и лекарственным абузусом эффективность СЗН была ниже, чем у пациентов без абузуса, перед началом инвазивного лечения пациент должен отказаться от приема этих средств, а при необходимости возможно проведение дезинтоксикационной терапии [53]. Наличие умеренных коморбидных психических нарушений (чаще всего депрессивно-тревожного спектра) не является критерием исключения для инвазивного вмешательства. У пациентов с личностными и соматоформными расстройствами применение любых методов НМ противопоказано [17].
Высказывается скептическое мнение о недоступности НМ для пациентов в связи с высокой стоимостью процедуры. В тоже время в одной из последних работ [54] метод НС определяется как экономически эффективная стратегии управления болью, позволяющая существенно улучшить качество жизни и работоспособность пациентов и в значительной степени снизить затраты на фармакотерапию, которую в течение многих лет вынуждены получать эти пациенты. Кроме того, в РФ в настоящее время действует программа квот для пациентов с некурабельными неврологическими болевыми синдромами.
Заключение.
Таким образом, методы высокотехнологичной нейромодуляции, как неинвазивной, так и инвазивной, в последние годы широко и успешно применяются для лечения тяжелых хронических первичных цефалгий, в первую очередь хронических форм мигрени и кластерной ГБ. Основным показанием для инвазивной НМ является рефрактерность цефалгического синдрома ко всем традиционным методам консервативного лечения (адекватная фармакотерапия, ботулинотерапия), а также неэффективность блокад периферических нервов и методов неинвазивной НМ. Для успешного применения методов НМ в лечении рефрактерных хронических цефалгий решающее значение имеет междисциплинарный подход с привлечением команды специалистов, имеющих опыт ведения таких пациентов и имплантации инвазивных устройств для НМ. Отбор пациентов, то есть оценка соответствия критериям рефрактерной ГБ и последующее послеоперационное наблюдение, должен осуществляться цефалгологом, предпочтительно на базе специализированного центра боли (головной боли). Анализ критериев включения для НМ и выбор индивидуальной, наиболее подходящей методики НМ является задачей нейрохирурга. Имплантация устройства должна осуществляться квалифицированной бригадой нейрохирургов, владеющих техникой имплантации инвазивных устройств для НМ.
При соблюдения этих условий методы высокотехнологичной НМ открывают перспективы существенного улучшения качества жизни у пациентов с тяжелыми хроническими цефалгиями, устойчивыми к другим видам лечения.
Литература
|
1. Minassian K., Hofstoetter U., Tansey K. et al. Neuromodulation
of lower limb motor control in restorative neurology.
Clin. Neurol. Neurosurg. 2012; 114 (5): 489–497.
doi: 10.1016/j.clineuro.2012.03.013. 2. Liberson W.T., Holmquest H.J., Scot D., Dow M. Functional electrotherapy: stimulation of the peroneal nerve synchronized with the swing phase of the gait of hemiplegic patients. Arch. Phys. Med. Rehabil. 1961; 42: 101–105. PMID: 13761879. 3. Shealy C.N., Mortimer J.T., Reswick J.B. Electrical inhibition of pain by stimulation of the dorsal columns: preliminary clinical report. Anesth. Analg. 1967; 46: 489–491. PMID: 4952225. 4. Cook A.W., Weinstein S.P. Chronic dorsal column stimulation in multiple sclerosis. Preliminary report. NY State J. Med. 1973; 73: 2868–2872. 5. DosSantos M.F., Ferreira N., Carvalho A.C., DaSilva A.F. Potential mechanisms supporting the value of motor cortex stimulation to treat chronic pain syndromes. Front. Neurosci. 2016; 10: 18. doi: 10.3389/fnins.2016.00018. 6. Шабалов В.А. Функциональная нейрохирургия. Лечение тяжелых болевых синдромов. Клиническая неврология. 2004; 3(2): 403–419. 7. Ghaly R.F., Tverdohleb T., Candido K.D., Knezevic N.N. Do we need to establish guidelines for patients with neuromodulation implantable devices, including spinal cord stimulators undergoing nonspinal surgeries? Surg. Neurol. Int. 2016; 7:18. doi: 10.4103/2152-7806.176373. 8. O’Neill F., Sacco P., Nurmikko T. Evaluation of a homebased transcranial direct current stimulation (tDCS) treatment device for chronic pain: study protocol for a randomised controlled trial. Trials. 2015; 16: 186. doi: 10.1186/ s13063-015-0710-5. 9. Осипова В.В., Филатова Е.Г., Артеменко А.Р. и др. Диагностика и лечение мигрени: рекомендации российских экспертов. Журнал неврологии и психиатрии имени С.С. Корсакова. 2017; 1(2): 28–42. doi: 10.17116/ jnevro20171171228-42. 10. Екушева Е.В., Артеменко А.Р., Осипова В.В. Современные аспекты диагностики рефрактерных форм первичной головной боли. Журнал неврологии и психиатрии имени С. С. Корсакова. 2017; 1(2): 48–53. doi: 10.17116/jnevro20171171248-53. 11. Kraus T., Kiess O., Hösl K. et al. CNS BOLD fMRI effects of sham-controlled transcutaneous electrical nerve stimulation in the left outer auditory canal – a pilot study. Brain Stimul. 2013; 6: 798–804. doi: 10.1016/j. brs.2013.01.011. 12. Beekwilder J.P., Beems T. Overview of the clinical applications of vagus nerve stimulation. J Clin. Neurophysiol. 2010; 27: 130–138. doi: 10.1097/WNP.0b013e3181d64d8a. 13. Сергеев А.В. Цервикогенная головная боль: доказательная диагностика и терапия. Мanage pain. 2017; 4: 16–19. 14. Lambru G., Matharu M.S. Peripheral neurostimulation in primary headaches. Neurol Sci. 2014; 35(1): 77–81. http://dx.doi.org/10.1007/s10072-014-1748-y. 15. Екушева Е.В. Оптимальные подходы к купированию приступа мигрени: прошлое, настоящее и будущее. Русский медицинский журнал. 2012; 10: 522–528. 16. Miller S., Matharu M. Non-invasive Neuromodulation in Primary Headaches. Curr. Pain Headache Rep. 2017; 21(3): 14. doi: 10.1007/s11916-017-0608-x. 17. Исагулян Э.Д., Осипова В.В., Екушева Е.В. и др. Нейромодуляция в лечении кластерной головной боли. Русский медицинский журнал. 2017; 24: С.1779-1784. 18. Sugiyama K., Nozaki T., Asakawa T. et al. The present indication and future of deep brain stimulation. Neurol. Med. Chir. (Tokyo). 2015; 55(5): 416–421. doi: 10.2176/ nmc.ra.2014-0394. 19. May A., Leone M, Boecker H. et al. Hypothalamic deep brain stimulation in positron emission tomography. J. Neurosci. 2006; 26: 3589–3593. doi: 10.1523/JNEUROSCI.4609-05.2006. 20. Dach F., Eckeli A.L., Ferreira K.S., Speciali J.G. Nerve block for treatment of headaches and cranial neuralgias – a practical approach. Headache. 2015; 55(1): 59–71. doi: 10.1111/head.12992. 21. Артеменко А.Р., Куренков А.Л., Антипова О.С., Никитин С.С. Нелекарственные методы лечения хронической мигрени. Диагностика и лечение хронической мигрени. М.: Горячая линия. Телеком, 2014: 141–153. 22. Lipton R.B., Pearlman S.H.Transcranial magnetic simulation in the treatment of migraine. Neurotherapeutics. 2010; 7(2): 204–211. https://doi.org/10.1016/j.nurt.2010.03.002. 23. Schwedt T.J., Vargas B. Neurostimulation for treatment of migraine and cluster headache. Pain Med. 2015; 16(9): 1827–1834. doi: 10.1111/pme.12792. 24. Gaul C., Diener H., Solbach K. et al. Quality of life in subjects treated by non-invasive vagus nerve stimulation using gammacore for the prevention and acute treatment of chronic cluster headache. J. Headache Pain. 2014; 15: 16. doi:10.1186/1129-2377-15-S1-I6. 25. Piquet M., Balestra C., Sava S.L. et al. Supraorbital transcutaneous neurostimulation has sedative effects in healthy subjects. BMC Neurol. 2011; 11: 135. doi: 10.1186/1471-2377-11-135. 26. Hong J., Ball P.A., Fanciullo G.J. Neurostimulation for Neck Pain and Headache. Headache. 2014; 54(3): 430–444. doi: 10.1111/head.12292. 27. Puledda F., Goadsby P.J. An update on non-pharmacological neuromodulation for the acute and preventive treatment of migraine. Headache. 2017; 57(4): 685–691. doi: 10.1111/head.13069. 28. Dasilva A.F., Mendonca M.E., Zaghi S. et al. tDCS-induced analgesia and electrical fields in pain-related neural networks in chronic migraine. Headache. 2012; 52: 1283– 1295. doi: 10.1111/j.1526-4610.2012.02141.x. 29. Brewer A.C., Trentman T.L., Ivancic M.G. et al. Longterm outcome in occipital nerve stimulation patients with medically intractable primary headache disorders. Neuromodulation. 2012. doi: 10.1111/j.1525-1403.2012.00490.x. 30. Chen Y.F., Bramley G., Unwin G. et al. Occipital nerve stimulation for chronic migraine — a systematic review and meta-analysis. PLoS ONE 2015; 10: e0116786. doi:10.1371/ journal.pone.0116786. 31. Kinfe T.M., Pintea B., Roeske S. et al. Percutaneous nerve field stimulation (PENS) of the occipital region as a possible predictor for occipital nerve stimulation (ONS) responsiveness in refractory headache disorders? A feasibility study. Cephalalgia. 2016; 36(8): 779–789. doi: 10.1177/0333102415613765. 32. Magis D., Gerard P., Schoenen J. Invasive occipital nerve stimulation for refractory chronic cluster headache: what evolution at long-term? Strengths and weaknesses of the method. J Headache Pain. 2016; 17: 8. doi: org/10.1186/s10194-016-0598-9. 33. Zach K.J., Trentman T.L., Zimmerman R.S., Dodick D.V. Refractory headaches treated with bilateral occipital and temporal region stimulation. Med. Devices (Auckl). 2014; 7: 55–59. doi: org/10.2147/MDER.S59719. 34. Lambru G., Matharu M.S. SUNCT and SUNA: Medical and surgical treatments. Neurol. Sci. 2013a; 34(1): 75–81. doi:10.1007/s10072-013-1366-0. 35. Leone M., Franzini A., D’Andrea G. et al. Deep brain stimulation to relieve drug-resistant SUNCT. Ann. Neurol. 2005; 57: 924-927. doi: 10.1002/ana.20507. 36. Láinez M.J., Martin A.S. Sphenopalatine ganglion stimulation in cluster headache and other types of headache. Cephalalgia. 2016; 36(12): 1149–1155. https://doi.org/10.1177/0333102416644968. 37. Jürgens T.P., May A. Role of sphenopalatine ganglion stimulation in cluster headache. Curr Pain Headache Rep. 2014; 18(7): 433. doi: 10.1007/s11916-014-0433-4. 38. Clelland C.D, Zheng Z., Kim W. et al. Common cerebral networks associated with distinct deep brain stimulation targets for cluster headache. Cephalalgia. 2014; 34(3): 224–230. http://dx.doi.org/10.1177/0333102413509431. 39. Schoenen J., Jensen R.H., Lantéri-Minet M. et al. Stimulation of the sphenopalatine ganglion (SPG) for cluster headache treatment. Pathway CH-1: a randomized, sham-controlled study. Cephalalgia. 2013; 33(10): 816–830. http://dx.doi.org/10.1177/0333102412473667. 40. Sillay K.A., Sani S., Starr P.A. Deep brain stimulation for medically intractable cluster headache. Neurobiol. Dis. 2010; 38(3): 361–368. doi:10.1016/j.nbd.2009.05.020. 41. Altinay M., Estemalik E., Malone DA. Jr. A comprehensive review of the use of deep brain stimulation (DBS) in treatment of psychiatric and headache disorders. Headache. 2015; 55(2): 345–350. doi: 10.1111/ head.12517. 42. Franzini A., Messina G. Surgery for treatment of refractory chronic cluster headache: toward standard procedures. Neurol. Sci. 2015; 36(1): 131–135. https://doi.org/10.1007/ s10072-015-2179-0. 43. Fontaine D., Lanteri-Minet M., Ouchchane L. et al. Anatomical location of effective deep brain stimulation electrodes in chronic cluster headache. Brain. 2010; 133(4): 1214–1223. PMID: 20237130. 44. Starr P.A., Barbaro N.M., Raskin N.H., Ostrem J.L. Chronic stimulation of the posterior hypothalamic region for cluster headache: Technique and 1-year results in four patients. J. Neurosurg. 2007; 106: 999–1005. doi:10.3171/ jns.2007.106.6.999. 45. Sillay K.A., Sani S., Starr P.A. Deep brain stimulation for medically intractable cluster headache. Neurobiol. Dis. 2010; 38: 361–368. doi: 10.1016/j.nbd.2009.05.020. 46. Walcott B.P., Bamber N.I., Anderson D.E. Successful treatment of chronic paroxysmal hemicrania with posterior hypothalamic stimulation: Technical case report. Neurosurgery. 2009; 65: E997. http://dx.doi.org/10.1227/01. NEU.0000345937.05186.73. 47. Lyons M.K., Dodick D.W., Evidente V.G. Responsiveness of short-lasting unilateral neuralgiform headache with conjunctival injection and tearing to hypothalamic deep brain stimulation. J. Neurosurg. 2009; 110: 279–281. doi: 10.3171/2008.4.17493. 48. The International Classification of Headache Disorders, 3rd edition (ICHD-3). Cephalalgia. 2018; 38(1): 1–211. doi: 10.1177/0333102417738202. 49. Leone M., Cecchini A.P. Central and Peripheral Neural Targets for Neurostimulation of Chronic Headaches. Curr. Pain Headache Rep. 2017; 21(3): 16. doi: 10.1007/s11916- 017-0616-x. 50. Martelletti P., Katsarava Z., Lampl C. et al. Refractory chronic migraine: a consensus statement on clinical definition from the European Headache Federation. J. Headache Pain. 2014; 15: 47. doi: 10.1186/1129-2377-15-47. 51. Mitsikostas D.D., Edvinsson L., Jensen R.H. et al. Refractory chronic cluster headache: a consensusstatement on clinical definition from the European Headache Federation. J. Headache and Pain. 2014, 15: 79. doi: 10.1186/1129-2377-15-79. 52. Leone M., May A., Franzini A. et al. Deep brain stimulation for intractable chron¬ic cluster headache: proposals for patient selection. Cephalalgia. 2004; 24: 934–937. doi: 10.1111/j.1468-2982.2004.00742.x. 53. Martelletti P., Jensen R.H., Antal A. et al. European Headache Federation. Neuromodulation of chronic headaches: position statement from the European Headache Federation. J. Headache Pain. 2013; 14: 86. doi: 10.1186/1129-2377-14-86. 54. Pietzsch J.B., Garner A., Gaul C., May A. Costeffectiveness of stimulation of the sphenopalatine ganglion (SPG) for the treatment of chronic cluster headache: a model-based analysis based on the Pathway CH-1 study. J. Headache Pain. 2015; 16: 48. doi: 10.1186/s10194-015-0530-8. |
1. Minassian K., Hofstoetter U., Tansey K. et al. Neuromodulation
of lower limb motor control in restorative neurology.
Clin. Neurol. Neurosurg. 2012; 114 (5): 489–497.
doi: 10.1016/j.clineuro.2012.03.013. 2. Liberson W.T., Holmquest H.J., Scot D., Dow M. Functional electrotherapy: stimulation of the peroneal nerve synchronized with the swing phase of the gait of hemiplegic patients. Arch. Phys. Med. Rehabil. 1961; 42: 101–105. PMID: 13761879. 3. Shealy C.N., Mortimer J.T., Reswick J.B. Electrical inhibition of pain by stimulation of the dorsal columns: preliminary clinical report. Anesth. Analg. 1967; 46: 489–491. PMID: 4952225. 4. Cook A.W., Weinstein S.P. Chronic dorsal column stimulation in multiple sclerosis. Preliminary report. NY State J. Med. 1973; 73: 2868–2872. 5. DosSantos M.F., Ferreira N., Carvalho A.C., DaSilva A.F. Potential mechanisms supporting the value of motor cortex stimulation to treat chronic pain syndromes. Front. Neurosci. 2016; 10: 18. doi: 10.3389/fnins.2016.00018. 6. Shabalov V.A. [Functional neurosurgery. Treatment of severe pain syndromes]. Klinicheskaya nevrologiya [Clinical neurology]. 2004; 3(2): 403-419. (In Russ.). 7. Ghaly R.F., Tverdohleb T., Candido K.D., Knezevic N.N. Do we need to establish guidelines for patients with neuromodulation implantable devices, including spinal cord stimulators undergoing nonspinal surgeries? Surg. Neurol. Int. 2016; 7:18. doi: 10.4103/2152-7806.176373. 8. O’Neill F., Sacco P., Nurmikko T. Evaluation of a homebased transcranial direct current stimulation (tDCS) treatment device for chronic pain: study protocol for a randomised controlled trial. Trials. 2015; 16: 186. doi: 10.1186/ s13063-015-0710-5. 9. Osipova V.V., Filatova E.G., Artemenko A.R. и др. [Diagnosis and treatment of migraine: recommendations of Russian experts]. Zhurnal nevrologii i psikhiatrii im. S.S.Korsakova. 2017; 1(2): 28–42. (In Russ.). doi: 10.17116/ jnevro20171171228-42. 10. Ekusheva E.V., Artemenko A.R., Osipova V.V. [Modern aspects of diagnosis of refractory forms of primary headache]. Zhurnal nevrologii i psikhiatrii im. S.S. Korsakova. 2017; 1(2): 48–53. (In Russ.). doi: 10.17116/jnevro20171171248-53. 11. Kraus T., Kiess O., Hösl K. et al. CNS BOLD fMRI effects of sham-controlled transcutaneous electrical nerve stimulation in the left outer auditory canal – a pilot study. Brain Stimul. 2013; 6: 798-804. doi: 10.1016/j. brs.2013.01.011. 12. Beekwilder J.P., Beems T. Overview of the clinical applications of vagus nerve stimulation. J Clin. Neurophysiol. 2010; 27: 130–138. doi: 10.1097/WNP.0b013e3181d64d8a. 13. Sergeev A.V. [Cervicogenic headache: evidence-based diagnosis and therapy]. Мanage pain. 2017; 4: 16–19. (In Russ.). 14. Lambru G., Matharu M.S. Peripheral neurostimulation in primary headaches. Neurol Sci. 2014; 35(1): 77–81. http://dx.doi.org/10.1007/s10072-014-1748-y. 15. Ekusheva E.V. [Optimal approaches to arresting a migraine attack: past, present and future]. RMZh. 2012; 10: 522–528. (In Russ.). 16. Miller S., Matharu M. Non-invasive Neuromodulation in Primary Headaches. Curr. Pain Headache Rep. 2017; 21(3): 14. doi: 10.1007/s11916-017-0608-x. 17. Isagulyan E.D., Osipova V.V., Ekusheva E.V. et al. [Neuromodulation in the treatment of cluster headache]. RMZh. 2017; 24: С.1779-1784. (In Russ.). 18. Sugiyama K., Nozaki T., Asakawa T. et al. The present indication and future of deep brain stimulation. Neurol. Med. Chir. (Tokyo). 2015; 55(5): 416–421. doi: 10.2176/ nmc.ra.2014-0394. 19. May A., Leone M., Boecker H. et al. Hypothalamic deep brain stimulation in positron emission tomography. J. Neurosci. 2006; 26: 3589–3593. doi: 10.1523/JNEUROSCI.4609-05.2006. 20. Dach F., Eckeli A.L., Ferreira K.S., Speciali J.G. Nerve block for treatment of headaches and cranial neuralgias – a practical approach. Headache. 2015; 55(1): 59–71. doi: 10.1111/head.12992. 21. Artemenko A.R., Kurenkov A.L., Antipova O.S., Nikitin S.S. Nelekarstvennye metody lecheniya hronicheskoj migreni. [Diagnosis and treatment of chronic migraine] М.: Hot line. Telekom, 2014: 141–153. (In Russ.). 22. Lipton R.B., Pearlman S.H.Transcranial magnetic simulation in the treatment of migraine. Neurotherapeutics. 2010; 7(2): 204-211. https://doi.org/10.1016/j.nurt.2010.03.002. 23. Schwedt T.J., Vargas B. Neurostimulation for treatment of migraine and cluster headache. Pain Med. 2015; 16(9): 1827–1834. doi: 10.1111/pme.12792. 24. Gaul C., Diener H., Solbach K. et al. Quality of life in subjects treated by non-invasive vagus nerve stimulation using gammacore for the prevention and acute treatment of chronic cluster headache. J. Headache Pain. 2014; 15: 16. doi:10.1186/1129-2377-15-S1-I6. 25. Piquet M., Balestra C., Sava S.L. et al. Supraorbital transcutaneous neurostimulation has sedative effects in healthy subjects. BMC Neurol. 2011; 11: 135. doi: 10.1186/1471-2377-11-135. 26. Hong J., Ball P.A., Fanciullo G.J. Neurostimulation for Neck Pain and Headache. Headache. 2014; 54(3): 430–444. doi: 10.1111/head.12292. 27. Puledda F., Goadsby P.J. An update on non-pharmacological neuromodulation for the acute and preventive treatment of migraine. Headache. 2017; 57(4): 685–691. doi: 10.1111/head.13069. 28. Dasilva A.F., Mendonca M.E., Zaghi S. et al. tDCS-induced analgesia and electrical fields in pain-related neural networks in chronic migraine. Headache. 2012; 52: 1283– 1295. doi: 10.1111/j.1526-4610.2012.02141.x. 29. Brewer A.C., Trentman T.L., Ivancic M.G. et al. Longterm outcome in occipital nerve stimulation patients with medically intractable primary headache disorders. Neuromodulation. 2012. doi: 10.1111/j.1525-1403.2012.00490.x. 30. Chen Y.F., Bramley G., Unwin G. et al. Occipital nerve stimulation for chronic migraine — a systematic review and meta-analysis. PLoS ONE 2015; 10: e0116786. doi:10.1371/ journal.pone.0116786. 31. Kinfe T.M., Pintea B., Roeske S. et al. Percutaneous nerve field stimulation (PENS) of the occipital region as a possible predictor for occipital nerve stimulation (ONS) responsiveness in refractory headache disorders? A feasibility study. Cephalalgia. 2016; 36(8): 779–789. doi: 10.1177/0333102415613765. 32. Magis D., Gerard P., Schoenen J. Invasive occipital nerve stimulation for refractory chronic cluster headache: what evolution at long-term? Strengths and weaknesses of the method. J Headache Pain. 2016; 17: 8. doi: org/10.1186/s10194-016-0598-9. 33. Zach K.J., Trentman T.L., Zimmerman R.S., Dodick D.V. Refractory headaches treated with bilateral occipital and temporal region stimulation. Med. Devices (Auckl). 2014; 7: 55–59. doi: org/10.2147/MDER.S59719. 34. Lambru G., Matharu M.S. SUNCT and SUNA: Medical and surgical treatments. Neurol. Sci. 2013a; 34(1): 75–81. doi:10.1007/s10072-013-1366-0. 35. Leone M., Franzini A., D’Andrea G. et al. Deep brain stimulation to relieve drug-resistant SUNCT. Ann. Neurol. 2005; 57: 924–927. doi: 10.1002/ana.20507. 36. Láinez M.J., Martin A.S. Sphenopalatine ganglion stimulation in cluster headache and other types of headache. Cephalalgia. 2016; 36(12): 1149–1155. https://doi.org/10.1177/0333102416644968. 37. Jürgens T.P., May A. Role of sphenopalatine ganglion stimulation in cluster headache. Curr Pain Headache Rep. 2014; 18(7): 433. doi: 10.1007/s11916-014-0433-4. 38. Clelland C.D, Zheng Z., Kim W. et al. Common cerebral networks associated with distinct deep brain stimulation targets for cluster headache. Cephalalgia. 2014; 34(3): 224–230. http://dx.doi.org/10.1177/0333102413509431. 39. Schoenen J., Jensen R.H., Lantéri-Minet M. et al. Stimulation of the sphenopalatine ganglion (SPG) for cluster headache treatment. Pathway CH-1: a randomized, sham-controlled study. Cephalalgia. 2013; 33(10): 816–830. http://dx.doi.org/10.1177/0333102412473667. 40. Sillay K.A., Sani S., Starr P.A. Deep brain stimulation for medically intractable cluster headache. Neurobiol. Dis. 2010; 38(3): 361–368. doi:10.1016/j.nbd.2009.05.020. 41. Altinay M., Estemalik E., Malone DA. Jr. A comprehensive review of the use of deep brain stimulation (DBS) in treatment of psychiatric and headache disorders. Headache. 2015; 55(2): 345–350. doi: 10.1111/ head.12517. 42. Franzini A., Messina G. Surgery for treatment of refractory chronic cluster headache: toward standard procedures. Neurol. Sci. 2015; 36(1): 131–135. https://doi.org/10.1007/ s10072-015-2179-0. 43. Fontaine D., Lanteri-Minet M., Ouchchane L. et al. Anatomical location of effective deep brain stimulation electrodes in chronic cluster headache. Brain. 2010; 133(4): 1214–1223. PMID: 20237130. 44. Starr P.A., Barbaro N.M., Raskin N.H., Ostrem J.L. Chronic stimulation of the posterior hypothalamic region for cluster headache: Technique and 1-year results in four patients. J. Neurosurg. 2007; 106: 999–1005. doi:10.3171/ jns.2007.106.6.999. 45. Sillay K.A., Sani S., Starr P.A. Deep brain stimulation for medically intractable cluster headache. Neurobiol. Dis. 2010; 38: 361–368. doi: 10.1016/j.nbd.2009.05.020. 46. Walcott B.P., Bamber N.I., Anderson D.E. Successful treatment of chronic paroxysmal hemicrania with posterior hypothalamic stimulation: Technical case report. Neurosurgery. 2009; 65: E997. http://dx.doi.org/10.1227/01. NEU.0000345937.05186.73. 47. Lyons M.K., Dodick D.W., Evidente V.G. Responsiveness of short-lasting unilateral neuralgiform headache with conjunctival injection and tearing to hypothalamic deep brain stimulation. J. Neurosurg. 2009; 110: 279–281. doi: 10.3171/2008.4.17493. 48. The International Classification of Headache Disorders, 3rd edition (ICHD-3). Cephalalgia. 2018; 38(1): 1–211. doi: 10.1177/0333102417738202. 49. Leone M., Cecchini A.P. Central and Peripheral Neural Targets for Neurostimulation of Chronic Headaches. Curr. Pain Headache Rep. 2017; 21(3): 16. doi: 10.1007/s11916- 017-0616-x. 50. Martelletti P., Katsarava Z., Lampl C. et al. Refractory chronic migraine: a consensus statement on clinical definition from the European Headache Federation. J. Headache Pain. 2014; 15: 47. doi: 10.1186/1129-2377-15-47. 51. Mitsikostas D.D., Edvinsson L., Jensen R.H. et al. Refractory chronic cluster headache: a consensusstatement on clinical definition from the European Headache Federation. J. Headache and Pain. 2014, 15: 79. doi: 10.1186/1129-2377-15-79. 52. Leone M., May A., Franzini A. et al. Deep brain stimulation for intractable chron¬ic cluster headache: proposals for patient selection. Cephalalgia. 2004; 24: 934–937. doi: 10.1111/j.1468-2982.2004.00742.x. 53. Martelletti P., Jensen R.H., Antal A. et al. European Headache Federation. Neuromodulation of chronic headaches: position statement from the European Headache Federation. J. Headache Pain. 2013; 14: 86. doi: 10.1186/1129-2377-14-86. 54. Pietzsch J.B., Garner A., Gaul C., May A. Costeffectiveness of stimulation of the sphenopalatine ganglion (SPG) for the treatment of chronic cluster headache: a model-based analysis based on the Pathway CH-1 study. J. Headache Pain. 2015; 16: 48. doi: 10.1186/s10194-015-0530-8. |